Ишемическая болезнь сердца (ИБС) является первойпо частоте причиной смерти во всем мире и в нашей стране[1]. Однолетняя смертность больныхс клинически выраженной сердечной недостаточностью (СН) достигает26–29 %, т. е. ежегодно в РоссийскойФедерации умирают от 880 до 986 тыс.больных СН [2].
Результаты крупных эпидемиологических исследований позволили установить, что частота сердечных сокращений (ЧСС) является независимымфактором риска, увеличивающимобщую смертность, частоту внезапной смерти и смертность от сердечно-сосудистых заболеваний (ССЗ) [3].
Среди лекарственных средств,использующихся в лечении ССЗ, только β-адреноблокаторы (БАБ), блокируя нейрогормональные системы,прежде всего симпато-адреналовую,способны снижать ЧСС и улучшатьпрогноз у пациентов с хроническойСН (ХСН) [4].
Применение БАБ ограничивается ихпобочными эффектами – артериальнойгипотонией, депрессией, эректильнойдисфункцией, атриовентрикулярнойблокадой, липидными нарушениями,неселективным влиянием на бронхии периферические сосуды. Это послужило предпосылкой к поиску новых препаратов, способных избирательноснижать ЧСС.
В 1979 г. DiFrancesco D. и Noble S.J.впервые описали в клетках синусового узла “F-каналы”. Их названиепроизошло от английского “funny”(“смешные, забавные”) благодаряналичию у них специфических, необычных свойств. К их числу относится,во-первых, способность к активациив период гиперполяризации клеточноймембраны, а не ее деполяризации, чтохарактерно для K+-токов. Во-вторых,активизация под воздействием циклических нуклеотидов вследствие прямого связывания с цАМФ, а не путем фосфорилирования каналов. В-третьих,наличие проницаемости для ионов как Na+, так и K+ [5].
Ивабрадин (Кораксан) – первыйпрепарат, действующий только начастоту сердечных сокращений, является избирательным и специфическимингибитором ионных токов If, уменьшающим скорость медленной спонтанной диастолической деполяризации. Снижая ЧСС, ивабрадин уменьшает потребность миокарда в кислороде и повышает доставку кислородак миокарду, что определяет показанияк его использованию при стенокардиинапряжения. Селективность действияна ЧСС в отсутствие отрицательногоинотропного эффекта позволяет сохранять сократимость миокарда, что особенно актуально в отношении пациентов с систолической дисфункцией [6].Антиангинальная и антиишемическаяэффективность ивабрадина была доказана в крупных рандомизированныхисследованиях с применением двойного слепого метода по сравнению
с плацебо, БАБ – атенололом и антагонистом кальция – амлодипином [7, 8].
В исследовании BEAUTIFUL(Morbidity-Mortality Evaluation ofthe If Inhibitor Ivabradine in Patients With Coronary Artery Disease and LeftVentricular Dysfunction), в которомоценивалась эффективность ивабрадина у больных ИБС и дисфункциейлевого желудочка (ЛЖ), ивабрадин посравнению с плацебо снизил ЧСС на6 уд./мин. Достоверных различий почастоте первичной комбинированной конечной точки (сердечно-сосудистаясмерть или госпитализация по поводу острого инфаркта миокарда – ИМ, развития или прогрессирования СН)
обнаружено не было. При запланированном анализе в подгруппе пациентов с исходной ЧСС > 70 уд./минивабрадин снижал частоту вторичныхконечных точек – госпитализаций поповоду фатального и нефатального ИМи потребности в коронарной реваскауляризации [9]. Однако возможностииспользования ивабрадина у пациентов со стабильной стенокардией (CC)и ХСН изучены недостаточно.
Цель исследования состояла в изучении особенностей ремоделированиясердца и сосудов у больных CC и ХСНишемического генеза на фоне комплексной терапии, включившей ивабрадин.
Материал и методы
В исследование были включены 78 пациентов с СС и симптомами ХСН, развившимися после перенесенного ИМ. Критерии включения:
• информированное согласие пациента на участие в исследовании;
• анамнез СС напряжения III–IVфункционального класса (ФК)в течение 3 месяцев до момента включения в исследование;
• наличие симптомов ХСН, развившихся после перенесенного ИМ,ЧСС > 70 уд./мин на фоне максимально переносимой дозы рекомендуемых БАБ.
Критерии исключения:
• гиперчувствительность к ивабрадину или к какому-либо из входящихв его состав дополнительных компонентов;
• нестабильная стенокардия;
• повторный ИМ в течение 3 месяцевперед исследованием;
• тяжелая почечная или печеночнаянедостаточность;
• синдром слабости синусового узла;
• синоатриальные блокады, атриовентрикулярные блокады 2–3-й степени;
• фибрилляция и трепетание предсердий;
• наличие пейсмекера.
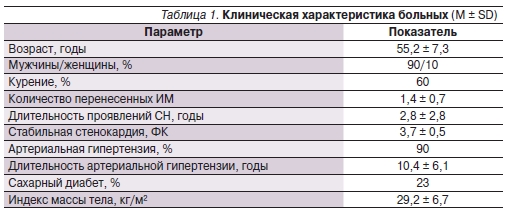
Обследовали 70 мужчин (90 %)и 8 женщин (10 %) в возрасте от 46 до67 лет, средний возраст – 55,2 ± 7,3года. Больше половины (60 %) больных курили. У обследованных пациентов среднее количество ИМ составило1,4 ± 0,7, длительность проявленийСН – около трех лет (2,8 ± 2,8 года),имелся высокий ФК СС – 3,7 ± 0,5.Артериальная гипертензия встречалась у 90 % пациентов, ее длительностьсоставила 10,4 ± 6,1 года. У 18 (22,5 %)больных имелся сахарный диабет типа 2. Индекс массы тела составил 29,2± 6,7 кг/м² (табл. 1).
Всем скринированным в исследование больным назначалась стандартная терапия в соответствии с Национальными рекомендациями по лечению СС и ХСН. В течение7–10 дней проводилась титрация дозыпрепаратов, в т. ч. рекомендуемыхБАБ, до максимально переносимой.Если на фоне терапии ЧСС оставалась > 70 уд./мин, пациент включалсяв исследование. Все больные, прошедшие скрининг, были рандомизированыв две группы. Пациентам (n = 40) первойгруппы к стандартной терапии добавляли ивабрадин (Кораксан; Лаборатория Сервье, Франция), пациенты (38больных) второй группы получалиобщепринятое лечение СС и ХСН.Ивабрадин назначали в начальнойдозе 5 мг (по 1 таблетке 2 раза в сутки)с последующей титрацией дозы. Одинраз в месяц посредством телефонного контакта осуществлялся контроль приема препаратов, титрации дозы,эффективности и переносимоститерапии.
Длительность лечения составила 6месяцев. Средняя доза ивабрадина входе титрации составила 5,25 ± 2,5мг/сут. В течение 6 месяцев наблюдения в каждой группе обследуемых90 % пациентов получали ингибиторыАПФ, 90 % – БАБ, 90 % – антиагреганты, 80 % – нитраты, 75 % – статины, 65 % – антагонисты альдостерона,25 % – диуретики.
Обследование осуществлено до начала терапии и через шесть месяцев лечения. Проба с дистанционной ходьбойв течение 6 минут проведена по стандартной методике [10]. Эхокардиографиявыполнена на комплексе Acuson 128XP/10. Использованы М-модальныйрежим, двумерный (В) режим, режимы импульсной и постоянно-волновойдопплерографии в стандартных эхокардиографических позициях. При оценкевариабельности ритма сердца (ВРС) осуществлен анализ во временных и спектральных областях. Использованыкороткие 5-минутные отрезки записи на аппарате фирмы “Волготех” [11].Для определения антитромбогенных(антикоагулянтных и фибринолитических) свойств стенки сосудов использована “манжеточная” проба, основанная на создании кратковременной(в течение 5 минут) ишемии путемналожения манжетки сфигмоманометра на плечо пациента и создания в нейдавления на 30 мм рт. ст. выше систолического, предложенная Балудой В.П.и соавт. [12]. Активность фактораВиллебранда определена по его способности вызывать агглютинациютромбоцитов в присутствии антибиотика ристомицина [13]. Для проведения данных исследований использованы наборы реагентов НПО “Ренам”.Исследование вазорегулирующейфункции эндотелия проведено в пробахс реактивной гиперемией и нитроглицерином [14]. Анализ пульсовой волнывыполнен с использованием оригинальной программы “Tensiomed” наартериографе “TensioClinic” (Венгрия)[15]. В динамике исследуемые параметры изучали у всех 78 больных.
Анализ данных осуществлен с помощью пакета прикладных программSTATISTICA 7.0. Использованы следующие методики статистического анализа: проверка нормальности распределения количественных признаков, описательная статистика, t-критерий Стъюдента для зависимых и независимых групп, критерий Вилкоксона для парных сравнений. Выборочные параметры, приведенные в таблицах, представлены в виде M (sd) или med (Lq; Uq), где M – среднее, sd – стандартное отклонение, med – медиана, Lq; Uq – межквартильный размах. Критическое значение уровня значимости принято равным 5 %.
Результаты
Не вызывает сомнения, что БАБ наиболее эффективны у пациентов с перенесенным ИМ по сравнению с другими группами препаратов, урежающихЧСС. Вместе с тем существует определенная категория больных, у которыхдобиться снижения ЧСС с помощьюадекватных доз БАБ не удается. Это может быть обусловлено симптомнойгипотонией или генетически обусловленным изменением чувствительностиβ-адренорецепторов к БАБ.
До лечения ЧСС у обследуемыхбольных составляла 74,6 ± 3,1 уд./мин.Через 6 месяцев терапии у пациентов,в составе комплексной терапии получавших ивабрадин, ЧСС была равной63,9 ± 3,2 уд./мин, что достоверно меньше исходной частоты (р < 0,01).Таким образом, ЧСС снизилась на 15 %. На фоне урежения ЧСС отмеченоуменьшение числа приступов стенокардии с 10,5 ± 8,5 до 5,8 ± 4,2 в неделю и потребности в нитроглицеринес 10,4 ± 8,6 до 5,6 ± 4,3 таблетки в неделю (р < 0,05). Таким образом, на фонекомплексной терапии, включившейивабрадин, число приступов стенокардии и потребность в нитроглицеринеуменьшились практически на 50 %.
У пациентов группы стандартной терапии через 6 месяцев произошло также достоверное урежение ЧСС до 69,3 ± 3,1 уд./мин по сравнению с исходными данными (р < 0,05), т. е. ЧСС уменьшилось на 7 %. Однако снижение ЧСС во второй группе пациентов было существенно меньше, чем у больных, принимавших ивабрадин в составе комплексной терапии (р < 0,05). На фоне стандартной терапии отмечено уменьшение числа приступов стенокардии с 10,3 ± 7,5 до 7,8 ± 4,1 в неделю и потребности в нитроглицерине с 10,4 ± 8,5 до 7,6 ± 4,2 таблетки в неделю (р > 0,05). На фоне стандартной терапии клиническое улучшение по данным показателям было менее выраженным и составило 30 %.
За период наблюдения отмечены стабилизация клинического состояния пациентов и уменьшение ФК ХСН. Так, у пациентов, получавших ивабрадин в составе комплексной терапии, на 25 % уменьшилось число больных с III и IV ФК ХСН. То есть у каждого четвертого больного с III и IV ФК ХСН повысилась переносимость физической нагрузки. В группе пациентов, получавших стандартную терапию, число таких больных уменьшилось на 10 %. Таким образом, у пациентов, получавших ивабрадин в составе комплексной терапии, толерантность к физической нагрузке повышается в большей степени (табл. 2).
Таблица 2. Изменение ФК ХСН и параметров сердца у больных СС и ХСН на фоне 6-месячной комплексной терапии, включившей ивабрадин (M ± sd).
Анализируя параметры эхокардиографии (ЭхоКГ) у пациентов, получавших в составе комплексной терапии ивабрадин, было выявлено увеличение УО ЛЖ с 79,2 ± 18,1 до 83,9 ± 18,9 мл, КДО ЛЖ с 199,1 ± 56,6 до 219,4 ± 54,0 мл (р < 0,05). ФВ ЛЖ при этом не изменилась и составила 38 %. У больных, получавших стандартную терапию, отсутствие значимого урежения ЧСС не привело к достоверным изменениям параметров ЭхоКГ.
Рисунок. Спектральный анализ вариабельности ритма сердца у больных СС и ХСН на фоне 6-месячной комплексной терапии, включающей ивабрадин.
Влияние 6-месячной комплексной терапии, включившей ивабрадин, на временные показатели ВРС было умеренным и заключалось в повышении общей мощности спектра (табл. 3). Это находило отражение в статистически значимом увеличении среднего значения всех RR-интервалов (Mean) c 871 (779; 920) до 957 (821; 1028) мс, среднего значения стандартных отклонений за 5-минутный период (SDNN-in) – с 714 (639; 754) до 785 (666; 843) мс. В группе больных, получавших стандартную терапию, достоверных изменений не установлено.
Таблица 3. Временной анализ вариабельности ритма сердца у больных СС и ХСН на фоне 6-месячной комплексной терапии, включившей ивабрадин, med (Lq; Uq).
Нами вывлено, что у больных СС и ХСН снижены низкочастотный компонент (LF) спектра, отражающий преимущественно симпатические влияния, высокочастотный компонент (HF) спектра, свидетельствующий о парасимпатическом воздействии на сердечный ритм, а также отношение низкочастотных волн к высокочастотным (LF/HF), представляющее уровень вагосимпатического баланса (см. рисунок). На фоне 6-месячной терапии отмечена тенденция к снижению симпатических влияний на сердечный ритм, однако не достигшему степени статистической достоверности в обеих группах обследуемых.
Таблица 4. Активность фактора Виллебранда, антикоагулянтная и фибринолитическая активность стенки сосудов эндотелияу больных СС и ХСН на фоне 6-месячной комплексной терапии, включившей ивабрадин, med (Lq; Uq).
Как видно из табл. 4, активность фактора Виллебранда у больных стабильной стенокардией и ХСН до лечения составила 178 %. Через 6 месяцев терапии в обеих группах медиана активности фактора Виллебранда составила 160 %, что свидетельствует о некотором снижении его активности. У больных СС и ХСН исходная активность антитромбина III снижена: до проведения манжеточной пробы
составила 90 %, после – 88 % (табл. 4). Через 6 месяцев терапии активность антитромбина III до и после манжеточной пробы увеличилась до 92 % (р < 0,05) в обеих группах обследуемых. Исходно и при повторном обследовании у больных преобладал патологический тип реакции эндотелия на кратковременную ишемию при проведении манжеточной пробы, характеризующийся отсутствием активации антитромбина III.
Начальное время фибринолиза до и после проведения манжеточной пробы составило 8, а через 6 месяцев терапии – 7 минут в обеих группах пациентов (р > 0,05; табл. 4).
У больных СС и ХСН существенной динамики сосудодвигательной функции эндотелия не установлено (табл. 5). По сравнению с практически здоровыми лицами у них повышена жесткость магистральных артерий (табл. 6). Скорость пульсовой волны в аорте (СПВА) составила 10,4 м/с, индекс аугментации аорты – 29,9 %, индекс аугментации плечевой артерии – 6,1 %. На фоне 6-месячной терапии указанные параметры существенно не изменились у больных обеих групп.
Обсуждение
Применение ивабрадина в комплексной терапии больных СС и ХСН сопровождается отчетливым антиангинальным действием, что подтверждается международными и российскими исследованиями [8, 9, 16]. Ивабрадин опосредует свое действие через урежение ЧСС. Снижение ЧСС вызывает уменьшение потребности миокарда в кислороде, а удлинение диастолы приводит к улучшению коронарной перфузии. Кроме того, доказана роль повышения ЧСС в прогрессировании коронарного атеросклероза [17].
В недавних экспериментальных исследованиях было продемонстрировано потенциальное значение селективного механизма снижения ЧСС ивабрадином при ХСН. При развитии ишемической СН на экспериментальной модели крыс длительное лечение ивабрадином приводило к постепенному снижению ЧСС при сохранении сердечного выброса за счет увеличения УО сердца. Отмечено значительное улучшение систолической функции ЛЖ за счет уменьшения его конечного систолического диаметра по сравнению с показателями нелеченых животных с СН. После 90 дней терапии ивабрадином наблюдалось снижение уровня норадреналина крови и улучшение морфологии ЛЖ. У леченных ивабрадином крыс отмечена меньшая плотность коллагена и увеличение плотности капилляров в сердечной мышце. Сохраняющийся эффект в течение 3 дней после отмены препарата, по мнению авторов, свидетельствует о благоприятном эффекте ивабрадина на ремоделирование левого желудочка [18]. Клиническим выражением функции миокарда является показатель сердечного выброса, вариабельность которого определяется двумя основными физиологическими детерминантами – ЧСС и УО. Как увеличение, так и поддержание адекватного сердечного выброса обеспечивается за счет модификации одного или обоих этих параметров. Любое состояние, приводящее к снижению насосной функции сердца, активирует оба эти механизма, через которые нейрогуморальная система старается поддерживать адекватное перфузионное давление, прежде всего в головном
мозге и почках.
Таблица 5. Вазорегулирующая функция эндотелия у больных СС и ХСН на фоне6-месячной комплексной терапии, включившей ивабрадин, med (Lq; Uq).
Таблица 6. Показатели жесткости артерий у больных СС и ХСН на фоне 6-месячнойкомплексной терапии, включившей ивабрадин, med (Lq; Uq).
В нашем исследовании отмечено снижение ЧСС на 10 ударов в минуту и увеличение УО ЛЖ на 5 мл, ФБ при этом не изменилась и составила 38 %. ФВ ЛЖ определяют как отношение УО к КДО, выраженное в процентах [19]. У обследуемых нами пациентов увеличение УО сопровождалось ремоделированием ЛЖ и увеличением КДО ЛЖ на 10 мл.
В целом благоприятное влияние комплексной терапии, включившей ивабрадин, на гемодинамику сердца проявлялось повышением толерантности пациентов к физическим нагрузкам. Так, у 25 % обследуемых пациентов 6-месячная терапия привела к улучшению ФК ХСН, что подтвердается данными литературы [20].
Еще в 1982 г. Bristow и соавт. показали, что важную роль в патогенезе ХСН играют гиперактивность адренергической системы и постоянно увеличивающийся уровень плазменных катехоламинов, которые могут усугублять миокардиальную дисфункцию за счет нарушений в сигнальной трансдукции и регуляции β-адренергических рецепторов со снижением их плотности в клетках миокарда. Эти данные легли в основу нейрогуморальной теории развития ХСН и определили стратегию снижения ЧСС как желаемую терапевтическую цель при лечении пациентов с этой патологией. Одним из методов оценки нейрогуморальных влияний на сердечно-сосудистую систему является определение ВРС.
Анализ результатов нашего исследования свидетельствует об умеренном влиянии комплексной терапии, включающей ивабрадин, на параметры ВРС после 6 месяцев наблюдения. Была выявлена тенденция к увеличению стандартного отклонения всех анализируемых RR-интервалов (SDNN), квадратного корня суммы разностей последовательных RR-интервалов (rMSSD), общей мощности спектра и спектра ультранизких частот. Увеличение этих параметров свидетельствует об уменьшении симпатического влияния на сердце. Необходимо также отметить, что увеличение SDNN составило 15 мс в условиях базовой терапии ингибиторами АПФ и БАБ. Для пациентов с ХСН это достаточно значимый результат, т. к., согласно данным исследования CHF-STAT, увеличение указанного параметра на 10 мс снижает риск смерти таких больных на 20 % [21].
Снижение сократительной способности миокарда ЛЖ приводит к развитию нарушений периферической гемодинамики, в т. ч. и дисфункции эндотелия [22]. Эндотелий представляет собой не просто барьер между потоком крови и гладкой мускулатурой сосудов, но является местом образования соединений, участвующих в процессах регуляции свертывания крови, сосудистого тонуса, функции тромбоцитов и развития сосудистой стенки [22]. Нарушение функции эндотелия способствует дальнейшему прогрессированию ХСН, снижению ФВ ЛЖ и развитию неблагоприятных сердечно-сосудистых событий, в т. ч. летальных исходов [23]. Нами выявлено, что 6-месячная комплексная терапии способствует снижению активности фактора Виллебранда до 160 % и повышению активности антитромбина III до 92 %. Эти результаты совпадают с данными литературы, свидетельствующими об улучшении антитромбогенной активности сосудистой стенки по мере уменьшения ФК ХСН [24].
Сосудодвигательная функция эндотелия была изучена в пробах с реактивной гиперемией и нитроглицерином. Систолическая дисфункция миокарда ЛЖ у пациентов с ХСН сопровождается нарушением сосудодвигательной функции эндотелия, причинами чего являются как недостаточный синтез факторов вазодилатации (оксид азота, эндотелиальный гиперполяризующий фактор, простациклин), так и избыточное образование вазоконстрикторов (ангиотензин II, эндотелин, свободные радикалы недоокисленных жирных кислот, простагландин F2α и тромбоксан А2) [25]. В течение 6 месяцев наблюдения нами не обнаружено достоверных изменений эндотелийзависимой и эндотелий-независимой вазодилатации.
Сокращение ЛЖ сердца генерирует пульсовую волну, которая распространяется вдоль артериальной стенки с определенной скоростью. Аорта и крупные артерии депонируют часть объема сердечного выброса во время систолы и восстанавливают его во время диастолы, тем самым обеспечивая непрерывность тока крови [26]. СПВА – центральное систолическое и пульсовое артериальное давление, индексы прироста – показатели жесткости артерий, использующиеся в настоящее время для оценки прогноза ССЗ [27]. В нашем исследовании на фоне 6-месячной терапии ивабрадином СПВА индексы аугментации аорты и плечевой артерии не изменились.
Анализ результатов 6-месячной комплексной терапии, включившей ивабрадин, показал хорошую переносимость этого препарата. У 2 (5 %) больных наблюдались фотопсии (преходящее усиление яркости в ограниченных участках зрительного поля). Этот феномен объясняется тем, что ивабрадин может взаимодействовать с Ih-ионными токами в сетчатке, схожими с If-токами в сердце и у некоторых пациентов может приводить к временным восприятиям за счет изменения реакции сетчатки на яркие световые стимулы [28, 29]. Однако фотопсии были умеренными и не стали поводом к отмене ивабрадина.
Заключение
Комплексная 6-месячная терапия у больных СС и ХСН, включающая ивабрадин, урежая ЧСС, способствует уменьшению числа приступов стенокардии напряжения и потребности в короткодействующих нитратах, повышению толерантности к физической нагрузке, замедлению процессов ремоделирования сердца и сосудов. Ивабрадин хорошо переносится; побочные эффекты встречаются в единичных случаях и не требуют прекращения приема препарата.


